- FORMAS ALOTROPICAS DEL CARBONO
Se conocen formas alotropicas del carbono que se conocen como:amorfa, grafito,diamante,fullerenos e isotopos.
DIAMANTE
A muy altas presiones, el carbono adopta la forma del diamante, en el cual cada átomo está unido a otros cuatro átomos de carbono, como en los hidrocarburos. El diamante presenta la misma estructura cúbica que el silicio y el germanio y, gracias a la resistencia del enlace químico carbono-carbono, es, junto con el nitruro de boro, la sustancia más dura conocida. La transición a grafito a temperatura ambiente es tan lenta que es indetectable. Bajo ciertas condiciones, el carbono cristaliza como lonsdaleíta, una forma similar al diamante pero hexagonal.

GRAFITO:
en este los atomos de carbono presenta hibridaciones sp2 esto significa que forma 3 enlaces covalentes en el mismo plano de 120 grados (estructura hexagonal) . el enlace covalente entre los atomos de capa es extremadamente fuerte sin embargo las uniones entre los diferente capas se realizan por fuerzas de ven der waals e interacciones entre orbitales y son mucho mas debiles esta estructura laminar hace que el grafito sea un material marcadamente anisotropo.
FULLERENO

Son la tercera formas mas estable del carbono despues del diamante y el grafito. Fueron recien y popularmente conocidos entre los quimicos tanto por su belleza estructural como su versaltilidad para la sintesis de nuevos compuestos, ya que se presntan en forma de esferas, cilindros . Los fullerenos esfericos reciben a menudo el nombre de buckyesferas y los cilindros de buckytubos o nanotubos.
AMORFA:
es una de las estructuras que pueden adoptar los materiales en estado solido. La estructura cristalina se presenta de forma de repeticion de subestructuras estrictamente periodocas , en las que domina en paralelismo , el cuarzo es el ejemplo mas habitual; por otra parte , en lo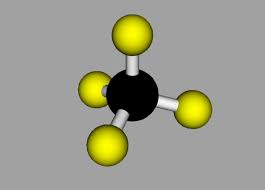 s cristales se distingue un orden a larga distancia, con una organizacion rigurosamente periodica de subestructuras en tanto que la estructuras amorfas, las subestructuras siguen lineas quebradas al azar y el orden solo se discierne a corta distancia. Los solidos amorfos difieren de los cristalinos por la manera en que se funden ; no tienen temperatura de fusion bien definida, se suavizan y se funden en un rango de temperatura y no tienen 'punto de fusion' .un solido amorfo consiste en particulas acomodadas en forma irregular y por ello no tienen el orden que se encuentra en los cristales. por ejemplos solidos amorfos son el vidrio y muchos plasticos.
s cristales se distingue un orden a larga distancia, con una organizacion rigurosamente periodica de subestructuras en tanto que la estructuras amorfas, las subestructuras siguen lineas quebradas al azar y el orden solo se discierne a corta distancia. Los solidos amorfos difieren de los cristalinos por la manera en que se funden ; no tienen temperatura de fusion bien definida, se suavizan y se funden en un rango de temperatura y no tienen 'punto de fusion' .un solido amorfo consiste en particulas acomodadas en forma irregular y por ello no tienen el orden que se encuentra en los cristales. por ejemplos solidos amorfos son el vidrio y muchos plasticos.
 s cristales se distingue un orden a larga distancia, con una organizacion rigurosamente periodica de subestructuras en tanto que la estructuras amorfas, las subestructuras siguen lineas quebradas al azar y el orden solo se discierne a corta distancia. Los solidos amorfos difieren de los cristalinos por la manera en que se funden ; no tienen temperatura de fusion bien definida, se suavizan y se funden en un rango de temperatura y no tienen 'punto de fusion' .un solido amorfo consiste en particulas acomodadas en forma irregular y por ello no tienen el orden que se encuentra en los cristales. por ejemplos solidos amorfos son el vidrio y muchos plasticos.
s cristales se distingue un orden a larga distancia, con una organizacion rigurosamente periodica de subestructuras en tanto que la estructuras amorfas, las subestructuras siguen lineas quebradas al azar y el orden solo se discierne a corta distancia. Los solidos amorfos difieren de los cristalinos por la manera en que se funden ; no tienen temperatura de fusion bien definida, se suavizan y se funden en un rango de temperatura y no tienen 'punto de fusion' .un solido amorfo consiste en particulas acomodadas en forma irregular y por ello no tienen el orden que se encuentra en los cristales. por ejemplos solidos amorfos son el vidrio y muchos plasticos.ISOTOPOS:
Son atomos de un mismo elemento que tienen igual numero de protones y electrones(igual numero atomico) pero diferente numero de neutrones(difiere en su masa atomica). los isotopos se denotan por el nombre del elemnto correspondiente seguido por el numero masico separados habitualmente por un guion ejm: carbono-12. si la relacion entre el numero de protones y neutrones no es la apropiada para obtener la estabilidad nuclear y este seria un isotopo radioactivo.Los isotopos son utilizados en la fotografia de rayos gamma en el cual se recoge la radiacion emitida y se obtiene una foto de la zona deseada.
GRUPOS FUNCIONALES ORGANICOS
El carbono es capaz de formar diversos grupos funcionales de acuerdo con el elemento con el cual este enlazado; debido a sus enlaces covalentes y su distribucion en el espacio se generaron diversos compuestos con caracteristicas similares a:
ALCANOS:
Son hidrocarburos con hibridacion SP3 formando moleculas con 109 grados. los alc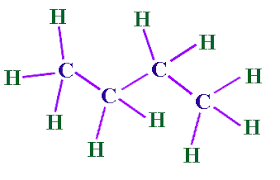 anos son insolubles en agua y los 4 primeros estan en estado gaseoso sus puntos de ebullicion y fusion varian de acuerdo con el nuemro de ramificaciones que tengan , la mayoria presentan enlaces covalentes debido a las cadenas consecutivas de carbono y su nomenclatura esta ligada a la cantidad de carbonos que tenga el compuesto.su formula es CnH2n+2 y se llama parafina.Las reacciones más importantes de los alcanos son la pirólisis,la combustión y la halogenación.
anos son insolubles en agua y los 4 primeros estan en estado gaseoso sus puntos de ebullicion y fusion varian de acuerdo con el nuemro de ramificaciones que tengan , la mayoria presentan enlaces covalentes debido a las cadenas consecutivas de carbono y su nomenclatura esta ligada a la cantidad de carbonos que tenga el compuesto.su formula es CnH2n+2 y se llama parafina.Las reacciones más importantes de los alcanos son la pirólisis,la combustión y la halogenación.

dependiendo del grupo funcional que este predominando se asigna un prefijo se asigna un sufijo para el caso de los alcanos sera el sufijo ANO.En el caso de una rama se utiliza el sufijo IL.
REGLAS PARA NOMBRAR UN ALCANO
1 Se busca la cadena de carbono consecutivos mas larga
2. Se enumera esta cadena buscando que las ramificaciones radicales queden mas cerca a los extremos de la cadena.
3.Se nombran las ramas de acuerdo con el grado de complejidad que tenga cada una se nombran desde las mas sencillas hasta las mas complejas
4. Se nombra la cadena mas larga asignando el sufijo ANO se llama rama o radical lo que quede afuera de la cadena.
PROPIEDADES Y USOS DE LOS ALCANOS
El estado físico de los 4 primeros alcanos: metano, etano, propano y butano es gaseoso. Del pentano al hexadecano (16 átomos de carbono) son líquidos y a partir de heptadecano (17 átomos de carbono) son sólidos.
El punto de fusión, de ebullición y la densidad aumentan conforme aumenta el número de átomos de carbono.
Son insolubles en agua
Pueden emplearse como disolventes para sustancias poco polares como grasas, aceites y ceras.
El gas de uso doméstico es una mezcla de alcanos, principalmente propano.
El gas de los encendedores es butano.
El principal uso de los alcanos es como combustibles
El estado físico de los 4 primeros alcanos: metano, etano, propano y butano es gaseoso. Del pentano al hexadecano (16 átomos de carbono) son líquidos y a partir de heptadecano (17 átomos de carbono) son sólidos.
El punto de fusión, de ebullición y la densidad aumentan conforme aumenta el número de átomos de carbono.
Son insolubles en agua
Pueden emplearse como disolventes para sustancias poco polares como grasas, aceites y ceras.
El gas de uso doméstico es una mezcla de alcanos, principalmente propano.
El gas de los encendedores es butano.
El principal uso de los alcanos es como combustibles
ALQUENOS:
Son compuestos que se identifican por la presencia de un doble enlace en su estructura, estan representados principalemente por los aceites , y algunos derivados del petroleo como la gasolina;su feormula general es CNH2N donde N es el numero de carbonos que tiene el compuesto . existen 2 clases de alquenos algunos alifaticos y aromaticos los primeros tiene forma de cadena y los siguientes estructuras en anillo mostrando capacidades de olor agradable con el pegante. Su nomenclatura es similar a la de los alcanos variando unicamente en la numeracion de la cadena del doble enlace debe quedar en la numeracion el mas cerca a las esquinas y la cadena principal lleva el sufijo ENO

Los alquenos son hidrocarburos con un doble enlace carbono-carbono. El doble enlace es un enlace más fuerte que el enlace sencillo, sin embargo, paradójicamente el doble enlace carbono-carbono es mucho más reactivo. A diferencia de los alcanos, que generalmente muestran reacciones más bien no específicas, el doble enlace es un grupo funcional en el que tienen lugar muchas reacciones con marcado carácter específico.
PROPIEDADES FISICAS
Las propiedades físicas de los alquenos son similares a las de los alcanos correspondientes. Los alquenos más pequeños son gases a temperatura ambiente. Comenzando por los compuestos C5, los alquenos son líquidos volátiles. Los alquenos isómeros tienen puntos de ebullición parecidos y las mezclas sólo pueden ser separadas mediante una destilación fraccionada realizada con mucho cuidado y con columnas de gran eficacia.
 ALQUINOS:
ALQUINOS:Son compuestos que se caracterizan por la presencia de un triple enlace entre carbono y carbono , su formula general CnH2n -2 donde n es el numero de carbono que tiene la dena principal el mas conocido de los alquinos es el acetileno el cual es usado para derretir metales y se conoce como soldadura autogena las moleculas de alquinos son moleculas lineales de 180 grados . Por consiguiente presenta poca rotacion y en el enlace triple es el mas fuerte en la clase de enlaces.

Su nomenclatura es identica a la de los alquenos si es de triple enlace la parate mas importante de la molecula quiere decir que al enumerar la cadena prima la presencia del triple enlace por encima del doble y de las ramas .
Se nombran terminando en -ino el nombre del alcano de igual número de carbonos. La numeración parte del extremo que permite asignar los localizadores más bajos al triple enlace.
PROPIEDADES FISICAS

Como podría esperarse,las propiedades físicas de los alquinos son muy similares a las de los alquenos y los alcanos.Los alquinos son ligeramente solubles en agua aunque son algo más solubles que los alquenos y los alcanos.A semejanza de los alquenos y alcanos, los alquinos son solubles en disolventes de baja polaridad,como tetracloruro de carbono,éter y alcanos.Los alquinos, al igual que los alquenos y los alcanos son menos densos que el agua.Los tres primeros alquinos son gases a temperatura ambiente.
Son compuestos que su estructura presenta un grupo funcional OH el cual significa grupo hidroxilo.
el grupo hidroxilo le da propiedades poalres generando cargas electricas negativas y positivas en la region del hidroxilo a diferencia de los otros 3 grupos que son apolares.
alcanos c=
alquenos c=
alquinos c=-

existen 3 clases de alcoholes primario cuando el carbono enlaza el OH esta enlazado a otro carbono c-c*-OH c* carbono primario
alcohol secundario cuando el carbono del grupo hidroxilo se encuentra unido a los dos carbonos
alcohol terciario cuando el carno del grupo hidroxilo se encuentra unidos a tres carbonos
PROPIEDADES DE LOS ALCOHOLES

Las propiedades físicas de un alcohol se basan principalmente en su estructura. El alcohol esta compuesto por un alcano y agua. Contiene un grupo hidrofóbico (sin afinidad por el agua) del tipo de un alcano, y un grupo hidroxilo que es hidrófilo (con afinidad por el agua), similar al agua. De estas dos unidades estructurales, el grupo –OH da a los alcoholes sus propiedades físicas características, y el alquilo es el que las modifica, dependiendo de su tamaño y forma.Densidad: La densidad de los alcoholes aumenta con el número de carbonos y sus ramificaciones. Es así que los alcoholes alifáticos son menos densos que el agua mientras que los alcoholes aromáticos y los alcoholes con múltiples moléculas de –OH, denominados polioles, son más densos.
PROPIEDADES QUIMICAS
Los alcoholes pueden comportarse como ácidos o bases, esto gracias al efecto inductivo, que no es más que el efecto que ejerce la molécula de –OH como sustituyente sobre los carbonos adyacentes. Gracias a este efecto se establece un dipolo.
La estructura del alcohol está relacionada con su acidez. Los alcoholes, según su estructura pueden clasificarse como metanol, el cual presenta un sólo carbono, alcoholes primarios, secundarios y terciarios que presentan dos o más moléculas de carbono.
Los alcoholes de peso molecular pequeños son liquidos y aquellos superiores a 8 carbonos son solidos su nomenclatura es similar a todos los compuestos alifaticos o de cadena pero los alcoholes priman la posicion de grupo hidroxilo OH sin que este dentro de la cadena las demas reglas cumplen de igual forma pero la cadena principal se le asigna el sufijo OL.
CICLO ALCANOS:
Son compuestos que forman anillos con sus cadenas de carbonos . pueden ser aromaticos o ciclicos de acuerdo con la cantidad de enlaces que tenga .
AROMATICOS:
Los compuestos ciclicos tienen como nomenclatura la misma que se utiliza en los alcanos anteponiendo al nombre principal la palabra ciclo , la cantidad de carbonos de la figura y el sufijo ANO ,ENO o INO.
cuando la cadena tiene mas carbonos que el anillo este se convertira en radical, cuando el anillo tiene mas carbonos que la cadena sera radical . Si existen dos radicales o ramas en el anillo se enumera tomando la rama mas sencilla como la del numero uno y las otras esten en numeros pequeños
BICICLOS:
Un biciclo son 2 ciclos unidos atraves de dos carbonos en un punto de enlace en los cuales son los que permiten las reacciones y union con otros compuestos. A estos se les llama policiclos y varian en su nomenclatura por que inician con la palabra biciclo, triciclo o policiclo ; para nombrarlo se escribe de ciclos que esten unidos .
ETERES:
Son compuestos derivados de los alcoholes que en la cadena principal incluyen un oxigeno, la mayoria de eteres son usados como disolventes o para estraccion de sustancias organicas provenientes de los vegetales por ejemplo: la clorofila y los agentes activos de la hoja de coca, marihuana y tabaco, su formula es R-O-R cada R la cantidad de cadenas de carbono que tiene el compuesto . para nombrar un eter, si su cadena principal se nombran ramas en orden de complejidad ubicadas a lado y lado del oxigeno y al final se les asigna la palabra eter. ejm: dimetil - eter.
cuando el eter es rama se utiliza el sufijo OXI y la cantidad de carbonos que estan unidos a el a nivel de complejidad es mas sencillo el eter que el alcohol.
ALDEHIDOS Y CETONAS:
Son compuestos derivados de la oxidacion de los alcoholes, se identifican con la presencia de un doble enlace con el oxigeno.
Su principal uso es el disolvente de sustancias organicas y la extraccion de agua permitiendo preservar tejidos durante un argo tiempo.
NOMENCLATURA
Para nombrar un aldehido se toman las mismas reglas que en la nomenclatura anterior pero el grupo funcional que predomina es el aldehido quiere decir que se enumera desde el carbono en donde esta formado este grupo funcional el resto de grupos funcionales iran como radicales o ramas in cluye la cetona, y la cadena principal se le asignara el sufijo AL o ALDEHIDO . Todas las ramas deben ser nombradas en orden de complejidad.
Para nombrar una cetona se pueden utilizar dos formas : la primera se toma como base el grupo funcional, nombrando los radicales como ramas seguidas de la palabra CETONA. el segundo metodo maneja la cadena mas larga , seguidos de la posicion de las cetonas y el sufijo ONA.

No hay comentarios:
Publicar un comentario